|
|
Átomo do Ouro
|
Fonte : http://7art-screensavers.com/screens/3d-atom-of-gold/3d-atom-of-gold-08.jpg |
 |
Fonte : http://pt.wikipedia.org/wiki/Lista_de_elementos_por_s%C3%ADmbolo
Nota : Mol é a unidade de medida de massa molecular, em que o Número de Avogadro é muito importante
( 1 mol = 6x10²³ moléculas) |
A teoria Atômica de Demócrito |
|
Demócrito foi um grande filósofo grego da escola que hoje classificamos como sendo da natureza. Era natural da cidade portuária de Abderam, na costa norte do mar Egeu. Nasceu no ano 460 a.C. e faleceu no ano 370 a. C..
“Demócrito concordava com seus antecessores num ponto : as transformações que se podiam observar na natureza não significavam que algo realmente “se transformava”. Ele presumiu, então, que todas as coisas eram constituídas por uma infinidade de pedrinhas minúsculas, invisíveis, cada uma delas sendo eterna e imutável. A estas unidades mínimas Demócrito deu o nome de átomos.
A palavra “átomo” significa “invisível”. Para Demócrito era muito importante estabelecer que as unidades constituintes de todas as coisas não podiam ser divididas em unidades ainda menores. Isto porque se os átomos também fossem passíveis de desintegração e pudessem ser divididos em unidades ainda menores, a natureza acabaria por se diluir totalmente. Como uma sopa que vai ficando cada vez mais rala.
Além disso, as “pedrinhas” constituintes da natureza tinham que ser eternas, pois nada pode surgir do nada. Neste ponto, Demócrito concordava com Parmênides e com os eleatas. Para ele, os átomos eram unidades firmes e sólidas. Só não podiam ser iguais, pois se todos os átomos fossem iguais não haveria explicação para o fato de eles se combinarem para formar de papoulas a oliveiras, do pêlo de um bode ao cabelo humano.
Demócrito achava que existia na natureza uma infinidade de átomos diferentes : alguns arredondados e lisos, outros irregulares e retorcidos. E precisamente porque suas formas eram tão irregulares é que eles podiam ser combinados para dar origem a corpos os mais diversos. Independentemente, porém, do número de átomos e de sua diversidade, todos eles seriam eternos, imutáveis e indivisíveis.
Se um corpo – por exemplo, de uma árvore ou de um animal – morre e se decompõe, seus átomos se espalham e podem ser reaproveitados para dar origem a outros corpos. Pois se é verdade que os átomos se movimentam no espaço, também é verdade que eles possuem diferentes “ganchos” e “engates” e podem ser novamente reaproveitados na composição de outras coisas que vemos ao nosso redor.
......................................................................................................................................................................
Hoje em dia podemos dizer que a teoria atômica de Demócrito estava quase perfeita. De fato, a natureza é composta por diferentes átomos, que se ligam a outros para depois se separarem novamente. Um átomo de hidrogênio presente numa célula da pontinha do meu nariz pode ter pertencido um dia à tromba de um elefante. Um átomo de carbono que está hoje no músculo do meu coração provavelmente esteve um dia na cauda de um dinossauro.
Hoje em dia, porém, a ciência descobriu que os átomos podem ser divididos em partículas ainda menores, as “partículas elementares”. São elas os prótons, nêutrons e elétrons. E talvez estas partículas também possam ser divididas em outras, menores ainda. Mas os físicos são unânimes em achar que em alguma parte deve haver um limite para esta divisão. Deve haver as chamadas partículas mínimas, a partir das quais a natureza se constrói.” (In “O Mundo de Sofia”, de Jostein Gaarder , Trad. João Azenha Jr., Ed. Cia das Letras, 46ª. ed.,2001, pp.57-59).
Do Renascimento aos nossos dias |
|
Muitos séculos se passaram desde Demócrito até que fosse formulada uma teoria atômica moderna. São descobertas importantes as seguintes :
Fissão nuclear:
Fontes :
http://www.geocities.com/SiliconValley/Lab/9043/quimica/resumo1.htm
http://pt.wikipedia.org/wiki/%C3%81tomo
http://www.if.ufrj.br/teaching/radioatividade/fnebomba.html
Noções Gerais no atual modelo |
|
Conceito : “O átomo é a menor porção em que pode ser dividido um elemento químico , mantendo ainda suas propriedades físico-químicas mínimas”. (In http://pt.wikipedia.org/wiki/%C3%81tomo )
Nomenclatura : o nome átomo é de origem grega – a (não) + tomos (parte) - , pois , quando foi descoberto, imaginava-se que não podia ser dividido. E assim lhe foi dado o nome com que Demócrito , filósofo grego da “escola da natureza”, no século V antes de Cristo, denominou a menor partícula que ele imaginava existente na natureza, que não comportava divisão. |
|

Átomo do Néon. Veja mais em :7art-screensavers.com/.../ 3d-atom-of-gold-08.jpg
|
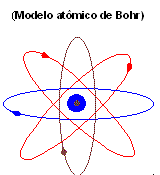 |
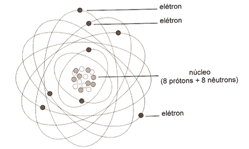
Partes : sabe-se hoje que os átomos são formados por duas partes : 1) o núcleo eletrônico, um núcleo onde se encontram prótons e nêutrons; 2 ) a eletrosfera, em torno do núcleo, onde se movimentam os elétrons , em órbitas elípticas.
Prótons : são partículas que compõem o núcleo de todo átomo, e possuem carga elétrica comumente entendida como positiva. |
|
Elétrons : são partículas que compõem o átomo e se encontram na eletrosfera, em constante movimento, desenvolvendo órbitas elípticas em torno do núcleo eletrônico, enquanto fazem rotação em torno de si mesmos. Possuem carga elétrica comumente entendida como negativa.
Nêutrons : são partículas que compõem o núcleo eletrônico do átomo e ficam junto aos prótons, não possuindo carga elétrica, mas detêm massa, sendo responsáveis pelo peso atômico e estabilizam o núcleo, visto que cargas elétricas iguais tendem a se repelir. |
 |
Spin : é o movimento de rotação do elétron em torno do seu eixo.
Camadas eletrônicas (ou níveis) : os elétrons estão distribuídos em camadas ou níveis de energia, representados graficamente pelas letras do alfabeto maiúsculas, de K a Q ou pelos números 1 a 7. Existe um número máximo de elétrons que pode ser contido em cada camada ou nível.
Orbital (ou sub-nível) : é uma região interna de espaço em torno do núcleo (eletrosfera) que pode tomar várias formas e onde é mais provável que esteja localizado um determinado elétron do átomo. O número máximo de elétrons em cada orbital é 2.
Carga Elétrica atômica : é a possuída pelas suas partículas, na proporção da tabelinha abaixo. O número de nêutrons é sempre o mesmo do de prótons. Se assim não fosse não haveria estabilidade nuclear.
Estado fundamental : o átomo está em seu estado fundamental quando eletricamente neutro, isto é, o mesmo número de prótons e de elétrons, para que haja a mesma carga negativa externa que a positiva interna, isto é, do núcleo - as cargas positivas e negativas, assim, são neutralizados pelos nêutrons .
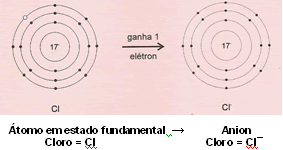
Íons : são átomos que não estão em seu estado fundamental, porque ganharam ou perderam elétrons. Quando ganham elétrons, chamam-se anions ( carga negativa) e quando perdem elétrons chamam-se cátions (carga positiva). Anions e cátions, no meio ambiente ou mediante operações laboratoriais, fazem
ligações entre a si para compensarem os elétrons faltantes, ou doar o excesso, formando moléculas e substâncias.
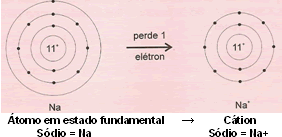
O número de elétrons que um átomo pode ganhar ou perder depende do tipo do átomo. Há átomos que perdem dois elétrons facilmente e se transformam em cátions com duas,três cargas positivas, etc.. O mesmo ocorre com os anions.Os átomos dos metais têm tendência para perder elétrons e, os dos não-metais, para ganhá-los.
No exemplo ao lado, o anion do Cloro (Cl¯) , que tem um elétron a mais pode fazer ligação com o cátion do Sódio (Na+) , que tem um elétron a menos e vão assim formar a substância Cloreto de Sódio (NaCl).
Outros exemplos : Ca²+ (cátion do Cálcio), O²¯( anion do Oxigênio). |
|
Número atômico : é um termo usado em física e química para designar o número de prótons no núcleo do átomo. Em um átomo em seu estado fundamental, ou seja, de carga neutra, o número de prótons = número de elétrons. Nos íons o número atômico ≠ número de elétrons. É o número atômico que caracteriza um elemento, convencionalmente ( e na Tabela Periódica) porque é estável. Não existe um elemento diferente do outro que possua o mesmo número atômico. Mesmo nos casos de fissão nuclear, quando se “quebra” o núcleo do átomo, o que ocorre é o aparecimento de outros elementos, diferentes do original. Isso quer dizer que, na realidade, o que caracteriza um elemento é o número de prótons existente no seu núcleo.
Massa atômica : é a massa do átomo e é igual à massa de prótons+ massa dos nêutrons. A massa do elétron é tão pequena que praticamente não precisa ser levada em conta. É mais ou menos 2.000 vezes menor que a massa da partícula positiva (é, precisamente, 1/1836 da massa do próton) . Os prótons têm massa e carga elétrica. Já os nêutrons têm massa, mas não têm carga elétrica. Por isso, na realidade, a massa do átomo é a soma das partículas positivas e neutras do átomo.
Elemento : denomina-se elemento químico todos os átomos que possuem o mesmo número atômico, ou seja, o mesmo número de prótons em seu núcleo. Os elementos químicos existentes e conhecidos são apenas aqueles relacionados na Tabela Periódica dos Elementos Químicos. Sua existência, descoberta e denominação é certificada pelo IUPAC - International Union of Pure and Applied Chemistry .
Substância química : com um pouco mais de 100 elementos químicos, pode-se formar milhares de substâncias químicas diferentes . Isso é possível porque os átomos podem se reunir, formando grupos chamados moléculas e grupos chamados aglomerados iônicos . Cada grupo (molécula ou aglomerado iônico) forma uma substância química.
Composto químico : é a substância química constituída por moléculas ou cristais de dois ou mais átomos ou íons ligados entre si, numa proporção fixa e definida. Exemplo : a água, que é formada de hidrogênio+oxigênio.
Isótopos : são átomos de um elemento químico cujos núcleos têm o mesmo número atômico mas diferentes massas atômicas. A palavra significa “no mesmo local” e faz alusão ao fato de que se situam no mesmo local da Tabela Periódica que o elemento com o mesmo nome. Na nomenclatura científica os isótopos são designados pelo nome do elemento químico seguido por um hífen e pela sua massa atômica –soma do número de prótons e nêutrons do seu núcleo atômico . Exemplos : ferro-57 (isótopo do ferro, que em seu estado fundamental tem 26 prótons e 30 nêutrons , massa atômica 56); urânio-235 (isótopo do urânio, que em seu estado fundamental tem 92 prótons e 145 nêutrons, massa atômica 238) e hélio-3 (isótopo do hélio, que em seu estado fundamental tem 2 prótons e 2 nêutrons, massa atômica 4).
Propriedades : são características especiais de cada elemento, que dependem de como se distribuem os elétrons nos níveis de energia de cada átomo - ou nas camadas mais externas, ou nas camadas mais internas, ou seja, diz respeito à configuração eletrônica. Quando a diferenciação advém da configuração eletrônica em um nível interno (ao menos um orbital “f” incompleto), o elemento se diz de transição interna (elementos dos períodos 6 e 7 do grupo 3, família 3B- os Lantinídios e os Actnídios) e, quando de um nível externo, diz-se de transição externa ou simplesmente de transição (ex. um íon que tenha uma orbital “d” incompleta com elétrons – vários metais, como o ouro, paládio, prata, titânio, etc.).
Ligações : átomos em situação de íons ( cátions ou anions) têm tendência a serem atraídos por outros, também com falta ou excesso de elétrons na última camada de sua eletrosfera, compensando-se mutuamente para completar o número total de elétrons idêntico ao do átomo do mesmo elemento em seu estado fundamental . Vão formar, assim, moléculas do mesmo elemento ou de outros elementos ou substâncias.
Fontes :
Telecurso 2000 – Ensino Médio – Química 2- da Fundação Roberto Marinho, Ed. Globo, 2002, pp.83-87
http://pt.wikipedia.org/wiki/Elemento_qu%C3%ADmico
pt.wikipedia.org/wiki/Átomo - 68k
http://www.calion.com/cultu/atomo/start.htm
7art-screensavers.com/.../ 3d-atom-of-gold-08.jpg
Notas de aula do Curso preparatório para Vestibular GPI, em 1995, em Copacabana, 1º semestre, Professores Marcos e Jeiel
|